臨床試験情報
JACCRO GC-09(研究代表者:伊澤 直樹)
| 項目 | 説明 |
|---|---|
| 試験課題名 | 切除不能進行・再発胃がんに対するナブパクリタキセルとラムシルマブ併用療法の隔週投与法における有効性と安全性を検討する第Ⅱ相試験 |
| 研究の目的 | 切除不能進行・再発胃癌に対するナブパクリタキセル(nab-paclitaxel:nab-PTX)の1コース目有害事象の出現程度を指標とした隔週(biweekly) nab-PTX+ラムシルマブ(ramcirumab:RAM)投与法への切り替えにおける安全性と有効性を評価する。 |
| Phase | PhaseⅡ |
| 適格規準 | 以下の規準を全て満たす症例を適格とする。 (1) ECOG performance status(PS)が0~1の症例 (2) 同意取得時の年齢が20歳以上の症例 (3) 評価可能病変を有する症例(RECIST Ver.1.1に基づく測定可能病変の有無は問わない) (4) 病理組織学的検査で胃腺癌または食道胃接合部腺癌であることが確認された症例 (5) 治癒切除不能な進行または再発の、胃または食道胃接合部癌の症例 (6) フッ化ピリミジン系薬剤を含む1次治療に不応・不耐となった症例。あるいは、フッ化ピリミジン系薬剤を含む術後補助化学療法中または術後補助化学療法の最終投与日から180日以内に再発が確認された症例 (7) 登録前7日以内の主要臓器機能について、以下の規準を満たしている症例 1)白血球数 12,000/mm^3以下 2)好中球数 1,500/mm^3以上 3)ヘモグロビン 8.0g/dL以上 4)血小板数 10.0×10^4/mm^3以上 5)総ビリルビン 施設基準値上限の1.5倍以下 6)AST 施設基準値上限の3倍以下(肝転移を有する場合は5倍以下) 7)ALT 施設基準値上限の3倍以下(肝転移を有する場合は5倍以下) 8)クレアチニン 施設基準値上限の1.5倍以下 9)蛋白尿(定性検査) 1+以下、または24時間蓄尿にて尿蛋白量が2g/24時間未満、または尿蛋白/クレアチニン比が2未満 10)PT-INR 施設基準値上限の1.5倍以下 11)aPTT 施設基準値上限の1.5倍以下 (8) 患者本人から文書による同意が得られている症例。 (9) 登録日より少なくとも90日以上の生存が期待できる症例 |
| 除外規準 | 以下の規準のいずれかに該当する症例は、本試験から除外する。 (1) 重度の薬物過敏症の既往歴がある症例 (2) 過去にタキサン系薬剤もしくは血管新生阻害薬が使用された症例 (3) 登録前14日以内に抗悪性腫瘍剤治療を受けた症例 (4) 登録前14日以内に輸血、血液製剤およびG-CSF等の造血因子製剤の投与を受けた症例 (5) 登録前28日以内に大手術(全身麻酔を必要とする手術等)を受けた症例 (6) 登録前28日以内に体腔液排除を必要する程度の多量の胸水、腹水または心嚢液貯留を認めた症例 (7) 同時性重複がんまたは無病期間が5年以内の異時性重複がんを有する症例。ただし、局所療法により治癒もしくは治癒相当と判断される上皮内がんまたは粘膜内がん相当の病変の場合は活動性の重複がんに含めない。 (8) 腹部を照射野に含む放射線治療、または腹部を透過する放射線治療を受けた症例 (9) 以下に該当する疾患の合併または既往がある症例 ・ 登録前28日以内に重篤または未回復の創傷、消化性潰瘍もしくは骨折がある ・ 登録前90日以内に、深部静脈血栓症、肺塞栓症、またはその他の重大な血栓症(静脈ポートまたはカテーテル血栓症もしくは表在性静脈血栓症は重大とみなさない)の既往がある ・ 登録前180日以内に消化管穿孔、瘻孔の既往がある ・ 登録前180日以内に心筋梗塞、不安定狭心症、脳血管発作、一過性脳虚血発作等を含む動脈血栓塞栓性関連事象の既往がある ・ 重大な出血障害または血管炎の合併がある、もしくは登録前90日以内に重大な消化管出血の既往がある ・ 症候性うっ血性心不全(New York Heart Associationによる心機能分類でクラスⅡ~Ⅳ)もしくは症候性またはコントロール不良の不整脈の合併がある ・ 標準的な医学的管理にもかかわらずコントロール不能の高血圧(収縮期血圧150mmHg以上,拡張期血圧90mmHg以上)の合併がある ・ 炎症性腸疾患または広範囲の腸切除(慢性下痢を伴う半結腸切除または広範囲の小腸切除)の既往または合併がある ・ 腸閉塞、クローン病、潰瘍性大腸炎または慢性下痢の合併がある ・ ヒト免疫不全ウイルス感染または後天性免疫不全症候群関連の疾患の合併がある ・ 重度の肺疾患(間質性肺炎,肺線維症等)、重度の肝疾患(肝硬変,肝不全等)の合併または既往がある,活動性の肝炎の合併がある ・ HBs抗原陽性である ・ Grade2以上の末梢性感覚ニューロパチーの合併がある ・ コントロールが困難な糖尿病の合併がある(ステロイドの使用に制限がある等) (10) ステロイド剤の継続的な全身投与(内服または静脈内)を受けている症例 (11) 処置を要する局所または全身性の治療が必要な活動性の感染症を有する症例(感染症に起因する38℃以上の発熱を認める患者等) (12) 広範な骨転移を有する(骨盤全体または脊椎の半分以上)症例 (13) 中枢神経系(脳、脊髄、髄膜)への転移を有する症例(臨床的な症状から中枢神経系への転移が疑われる場合は登録前にCTまたはMRIで中枢神経系への転移の有無を確認すること) (14) ワルファリン、低分子ヘパリン等の抗凝固療法を受けている症例(ただし、予防目的で低用量抗凝固療法を受けている場合は除く) (15) 他の抗血小板薬(クロピドグレル、チクロピジン、ジピリダモール、アナグレリド等)の長期投与を受けている(325mg/日までのアスピリンは使用可とし、疼痛に対する非ステロイド性抗炎症薬の使用は含まない) (16) 精神障害または精神症状を合併しており本研究への参加が困難と判断される症例 (17) 避妊する意思のない男性、および、妊婦、授乳婦、妊娠検査陽性の女性または避妊する意思のない女性 (18) その他、研究責任医師または研究分担医師が本研究の対象として不適当と判断した症例 |
| Regimen |
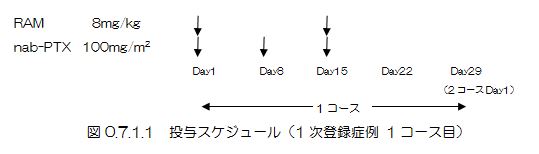
1次登録症例 <本登録規準>
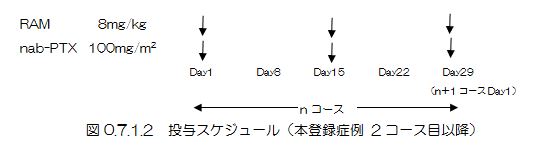
本登録症例
4週間を1コースとして、「10 被験者ごとのプロトコール治療中止規準」に達するまで、これを繰り返す。 |
| 評価項目 | 主要評価項目:無増悪生存期間(progression-free survival:PFS) 副次評価項目:全生存期間(overall survival:OS)、奏効割合(response rate:RR)、病勢制御割合(Disease control rate:DCR)、有害事象の発生割合(1コース目/2コース目以降)、relative dose intensity(全体/2コース目以降)、QOL |
| 目標症例数 | 66例(うち、本登録症例40例) |
| 研究期間 | 登録期間:2019年1月~2020年12月(2年) 追跡期間:最終症例登録終了後1年間 試験期間:2019年1月~2021年12月(3年) |